ソース:Dovepress 科学・医学研究へのオープンアクセス
Novel oral antivirals in hospitalized COVID-19 patients | CLEP (dovepress.com)
以下、機械翻訳です。
中華人民共和国の最初の付属病院で、COVID-19の入院患者 36件のRCTを含む33,555人の患者データを分析。
36件の研究、33,555人を7つの新規経口抗ウイルス薬に無作為に割り付けたものである。
方法:2022年11月30日までの入院中のCOVID-19患者の治療薬として、
バリシチニブ、
イベルメクチン(IVM)、
ファビピラビル(FVP)、
クロロキン(CQ)、
ロピナビルおよびリトナビル(LPV/RTV)、
ヒドロキシクロロキン(HCQ)、
ヒドロキシクロロキンとアジスロマイシンの併用(HCQ+AZT)を
含む新規経口抗ウイルス薬の有効性と安全性に関するランダム化臨床試験(RCT)。
結論
要約すると、現在推奨されている抗ウイルス薬であるバリシチニブ、IVM(イベルメクチン)、およびFVP(ファビピラビル)は、入院中のCOVID-19患者の疾患進行予防のために継続する必要があります。これらの知見は、新たな変異株によって引き起こされる感染の波に対処するための公衆衛生対策と、ウイルスの進化に対抗するための新しい経口抗ウイルス薬の開発の重要性を浮き彫りにしている。このNMAには、当時利用可能な最高レベルの確実性が含まれていましたが、研究者にとって透明性を高めるためにデータを共有することが不可欠でした。RCTから得られた個々の患者データのメタアナリシスは、患者の特性に基づいて治療を調整するための次の論理的なステップとなる。
英文だったので、ブラウザ機能で自動翻訳したものが以下です。
=====
全文翻訳
劉 浩双1,2陳景峰(Jingfeng Chen)1,2ウェイハオ・シャオ、3蘇燕、1,2スーイン・ディン1,2
1健康管理センター、鄭州大学、鄭州、450052、中華人民共和国の最初の付属病院。2公衆衛生学院、鄭州大学、鄭州、450001、中華人民共和国;3人口医学および公衆衛生の学校、中国医学科学院および北京連合医科大学、北京、100730、中華
人民共和国 対応:Suying Ding、健康管理センター、鄭州大学第一附属病院、龍虎中環路、金水区、河南省、450052、中華人民共和国、電話+86 158 3802 3097、電子メール fccdingsy@zzu.edu.cn
目的:現在、2019年のコロナウイルスパンデミック(COVID-19)の治療のために、多数の薬理学的介入が研究されており、その証拠は急速に進化しています。私たちの目的は、これらの薬の有効性と安全性の比較を評価することです。
方法:2022年11月30日までの入院中のCOVID-19患者の治療薬として、バリシチニブ、イベルメクチン(IVM)、ファビピラビル(FVP)、クロロキン(CQ)、ロピナビルおよびリトナビル(LPV/RTV)、ヒドロキシクロロキン(HCQ)、ヒドロキシクロロキンとアジスロマイシンの併用(HCQ+AZT)を含む新規経口抗ウイルス薬の有効性と安全性に関するランダム化臨床試験(RCT)を検索した。このネットワークメタアナリシス(NMA)の主なアウトカムは、院内死亡率、有害事象(AE)、回復時間、末梢毛細血管酸素飽和度(SpO2)の改善であった。二値の結果については、オッズ比(OR)を使用し、95%信頼区間(CI)を決定した。また、メタ回帰を用いて、異なる治療法が有効性と安全性に影響を与えるかどうかを調べた。STATA 15.0 は NMA の実施に使用されました。研究計画書はPROSPERO(#CRD 42023415743)に登録されました。
結果:COVID-19の入院患者33,555例を対象とした36件のRCTを本解析に組み入れた。まず、さまざまな新規経口抗ウイルス薬の有効性を比較した。バリシチニブ(OR 0.56, 95% CI: 0.35〜0.90)は、院内死亡率の低下において最適なプロバイオティクス種である可能性が最も高いことを示し、プラセボよりも優れた有害事象を減少させる介入はなかったことが示唆された。安全性アウトカムに関しては、IVMはCOVID-19入院患者の回復時間の改善で第1位にランクされました(平均差(MD)-1.36、95%CI:-2.32〜-0.39)。さらに、患者はSpO2を増加させる可能性が最も高い(OR 1.77、95%CI:0.09〜3.45)。メタ回帰分析では、COVID-19入院患者のすべての転帰において、異なる新規経口抗ウイルス薬を使用した参加者間に有意差は認められなかった。
結論:現在、バリシチニブはCOVID-19入院患者の院内死亡率を低下させており、エビデンスの確実性は中等度である。IVMは回復時間の改善においてプラセボよりも安全な選択肢であるように思われ、FVPはSpO2の安全性アウトカムの増加と関連していた。これらの予備的な証拠に基づく観察は、より多くのデータが公開されるまでの臨床診療の指針となるはずです。
キーワード: COVID-19, ネットワークメタアナリシス, 薬理学的介入, 有効性, 安全性
紹介
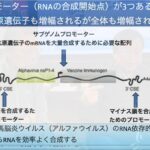
2019年のコロナウイルスパンデミック(COVID-19)の世界的な影響は甚大です。世界保健機関(WHO)は、2022年11月28日現在、6,608,893人の死亡を含む637,404,847人のCOVID-19の確定症例を報告しています。1、2COVID-19は、2019年後半に新たに発見された重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)のパンデミックです。3感染者の呼吸器系は、SARS-CoV-2の飛沫やエアロゾルの感染経路として機能します。4この病気は、軽度のインフルエンザのような症状から、より重篤な急性呼吸窮迫症候群まで、さまざまな症状を示し、最終的には死に至ります。5一本鎖RNAウイルスであるSARS-CoV-2は、スパイクタンパク質の結合を介してACE2受容体を介して侵入します。6複製プロセスでは、RNA依存性RNAポリメラーゼを使用して新しいウイルス粒子の合成を促進し、宿主細胞から脱出して隣接する細胞で複製サイクルを開始します。7COVID-19に罹患した患者の臨床転帰を高め、寿命を延ばすために、多くの治療薬がレビューされています。
COVID-19との闘いは、急性疾患のスクリーニングと管理だけでは終わらないようです。新型コロナウイルス感染症(COVID-19)の世界的な流行は3年が経過しています。何百万もの症例から得られた証拠は、COVID-19の症状が最初の急性期をかなり過ぎてからかなりの数の人々に発生する可能性があることを示しています。この状態は、COVID-19急性後遺症またはlong COVIDと呼ばれます。8long COVIDの症状は不均一であり、単一の疾患現象ではなく、多症候性および多段階性であることを示しています。患者は数週間から数か月にわたってさまざまな症状を経験することが多く、最初の診断から2年間苦しみ続ける人もいます。症状は蔓延しており、多系統の関与を示唆し、患者の生活の質に悪影響を及ぼします。9新たなエビデンスは、症状の一部が時間の経過とともに解消することを示唆しているが、多くは感染後6カ月経過しても人生を変えるような症状に苦しみ続けている。10したがって、long COVID治療薬の開発を加速させるためには、まず危険因子を特定し、次に原因を特定して理解することが重要です。
COVID-19に対するワクチンが開発され、広範な予防接種キャンペーンも行われています。Zambia Researchによると、COVID-19ワクチンはCOVID-19感染者の死亡率を大幅に低下させる可能性があります。112022年11月23日現在、中国では34億7,000万回分以上の新型コロナウイルスワクチンが接種されています。12安全で効果的なCOVID-19ワクチンが待ち望まれています。ワクチンの有効性とともに、ワクチンの普及はCOVID-19の蔓延を緩和する上で極めて重要な役割を果たします。13ワクチンは安全であると考えられているにもかかわらず、ワクチン忌避は予防接種率を上げる上で大きな障害となっています。14WHOが2019年に発表した世界の健康に対するリスクトップ10の1つは、ワクチン忌避です。15ワクチン忌避は、さまざまな要因から生じます。疾患リスクの認識、ワクチンの安全性に関する懸念、施設や医療従事者への信頼(不信)、さまざまな社会人口統計学的特性(年齢、性別、収入、教育レベルなど)はすべて、ワクチンの受容または拒否の重要な決定要因であることが以前の研究で示されています。16、17 しかし、ワクチンを接種した人でも新型コロナウイルスの変異株に感染する可能性があるという研究結果が出ています。免疫力が低下している人のかなりの数がワクチン接種後に十分な防御を受けられない可能性があり、現在のワクチンでは新型コロナウイルスの新興型に対して十分な効果が得られない可能性があるという潜在的な懸念があります。18そのため、簡便なコロナウイルスの経口治療薬の開発が不可欠です。
最近の経口コロナウイルス治療薬を用いた臨床試験では、良好な結果が得られています。この世界的な健康上の大惨事に対応して、数多くの抗ウイルス薬、免疫療法、ワクチンが試験されていますが、COVID-19を治療または予防するためのランダム化臨床試験(RCT)で有効性を示したものはほとんどありません。経口抗ウイルス薬は、SARS-CoV-2やレムデシビル(RDV)の静脈内投与に対するモノクローナル抗体よりも投与が容易な選択肢です。COVID-19の臨床試験では、コルチコステロイド、トシリズマブ、ヒドロキシクロロキン(HCQ)、およびロピナビルとリトナビルの併用(LPV/RTV)、イベルメクチン(IVM)、ファビピラビル(FVP)などの抗ウイルス薬が検討されています。19–22これらの科学的努力にもかかわらず、治療法に関する決定的なコンセンサスはまだ不足しています。
COVID-19の入院患者の治療における有効性と安全性の観点から、7種類の新規経口抗ウイルス薬を比較したすべてのRCTの概要を報告する。直接比較(RCTで治療を評価する場合)および間接比較(一般的な比較治療と比較して治療がどの程度有効であるかの結果を組み合わせて試験間で治療を比較する場合)のデータを含めることができるネットワークメタアナリシス(NMA)を採用した。通常の臨床診療では、臨床医は複数の治療オプションにアクセスでき、各患者に最適な治療法を選択するために確固たるエビデンスに頼らなければなりません。したがって、NMA所見の臨床的に関連する要約が提示され、治療の決定に情報を提供するために使用できます。
メソッド
このシステマティックレビューとNMAは、システマティックレビューおよびメタアナリシス(PRISMA)の報告ガイドライン(表S1)に従って実施されました。23研究計画書は、International Prospective Register of Systematic Reviews(PROSPERO)(#CRD 42023415743)に登録されました。
検索戦略
PubMed、Web of Science、Embase、およびコクラン・ライブラリを、開始から2022年11月30日まで検索した。これらの研究はすべて、2020年から2022年の間に英文ジャーナルに掲載された。電子データベースを検索する際には、自由語と主語の組み合わせを使用しました。完全な検索戦略は、表 S3 に記載されています。
研究の選択
COVID-19の入院患者に治療として経口抗ウイルス薬を投与したすべてのRCTを、開始から2022年11月30日までに選択対象として検討した。年齢、性別、人種、民族、治療期間の制限はなかった。症例報告、会議抄録、横断研究および観察研究、単群研究、およびヒト以外の研究は除外した。
LHSとCJFは、独立した研究調査を実施し、EndNote 20で見つかったすべての論文のタイトルと抄録を評価しました。得られた研究は、同じ査読者による全文の包括的なレビューを通じて適格性を評価した。LHSとCJFは、すべての問題を解決することで合意に達しました。重複した結果は、LHSによるEndNote 20の参照インポート時に削除されました。手動削除を使用して、残りの重複を削除しました。
成果指標
主要アウトカムは院内死亡率であった。副次アウトカムは、有害事象(AE)、回復時間、またはSpO2の改善とした。
主要アウトカムは、死亡が28日目の前後に発生したかどうかにかかわらず、院内死亡率(すなわち、初回入院中の死亡、退院時の追跡調査の中止)に対する影響を評価することであった。回復時間(患者が登録から28日以内に8つのカテゴリーの序数尺度でカテゴリー1、2、または3を達成した最初の日)は、副次的アウトカム指標であった。SpO2 は、臨床モニタリング プロトコルに従って校正されたパルス オキシメーターを使用して測定されました。重症度に関係なく、すべてのAEが記録され、分析に含められました。
データ解析
STATA(STATA Corp, College Station, Texas, United States of America, version 15.0)およびR(version 4.2.2)ソフトウェアを用いて、頻度論的フレームワークでランダム効果NMAを実施した。24直接的および間接的(および混合)の比較は、STATAの自己プログラムルーチンを使用して行われました25と R の bugsnet パッケージ。26効果は、二値変数のオッズ比(OR)および連続変数の平均差(MD)で推定され、いずれも95%信頼区間(CI)であった。関心のある連続変数の中央値(四分位範囲)が提示されたとき、計算によって平均(標準偏差)に変換されました。270.05未満の両側p値は統計的に有意であると見なされました。
NMAはSTATA 15.0を用いて実施した。ランダム化を維持しながら直接的および間接的な証拠をプールする頻度主義的アプローチを使用して、STATA の “mvmeta”、”mvmeta-make”、および “network” パッケージを使用してランダム効果モデルを実施しました。直接的証拠は、(従来のメタアナリシスと同様)RCTに基づくプール効果を指し、間接的証拠は、A-v-BおよびA-v-Cから外挿されたネットワーク、例えば、BおよびCの差から計算される。
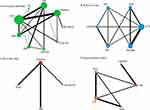
ネットワークごとにネットワーク マップが生成されました。NMAは、各介入間の直接的および間接的なエビデンス、ならびにCIおよびp値(0を除いた95%CIとして計算)に基づいて、群間MD効果量を提供する。Cohen の d 解釈は、効果サイズを記述するために使用されました。小0.2、中0.5、大0.8。
治療戦略は、累積ランキング曲線 (SUCRA) 確率の下で各結果の表面によってランク付けされます。各シミュレーションでSUCRAの確率が高いほど、最適な治療レジメンである可能性が高くなります。
バイアスのリスク
研究方法論の評価には、コクラン共同計画のバイアスリスクツールを用いた。試験でバイアスのリスクが高い(ROB)可能性が高い成分の数を用いて、試験をROBの3つのカテゴリー(高リスク、中等度リスク、低リスク)に分類した。28意見の相違点は、合意に達するまで話し合いによって解決されます。RevMan 5.3を使用して、リスクサマリーとバイアスリスクマップを作成しました。
追加解析
STATA 15.0研究における漏斗プロットの視覚的分析は、出版バイアスを評価するための一次および二次アウトカムに寄与する(図S4)。有意な不整合がある場合には、アウトカム評価の異なる取り扱いを考慮したメタ回帰分析が必要であった(表S4)。てこ比プロットは、てこ比値が高いとモデル全体に大きな影響を与える可能性があるため、研究の各結果における異質性の有意性を評価するのに役立ちます。てこ比プロットが低異質性を示している場合、つまり、ほとんどのデータポイントのてこ比値が比較的低い場合、その研究の均質性は良好であり、研究の異質性が低いことを示すと見なすことができます(比較調整されたファネルプロットは、出版バイアスを評価するために構築され、ファネルの非対称性はエッガーの検定を使用してテストされました)。
業績
選択した研究の特徴
本研究の検索方法を用いた初期検査で、合計4,813件の適格な研究が同定された。適格と考えられる1,392件の研究の全文は、タイトルと抄録をスクリーニングし、重複を削除した後に検索した。全体として、2020年から2022年にかけてNMAに36件のRCTを使用した(表S5)。33,000人、500人、55人が7つの新規経口抗ウイルス薬(バリシチニブ、IVM、FVP、CQ、LPV/RTV、HCQ、またはHCQ+AZT)のいずれかにランダムに割り付けられ、NMAに組み入れられた。図1は、体系的な文献検索と研究選択のプロセスを示しています。表 S2 に、試行の特性を示します。
 |
図 1選択方針のフロー図。 注:検索フロー図は、ネットワークメタアナリシスに最終的に含まれた論文の検索、スクリーニング、検索、および評価をまとめたものです。 |
バイアスのリスク
主要アウトカムおよび副次アウトカムに寄与する研究における出版バイアスの結果を図S1に示し、バイアスのリスクは圧倒的に低い(図S2)。詳細情報は、表S5に提供される。
ネットワークメタアナリシス
バリシチニブ試験に登録された患者数は1,315人で、男性が圧倒的に多かった。バリシチニブの最も定期的に処方される用量は4mg /日で、14日間経口投与されます。バリシチニブは主にプラセボと比較された。追跡期間は、いくつかのバリシチニブ研究で28日から60日の間で異なっていた。一方、IVM試験に登録された患者数は1,069人で、男性が圧倒的に多かった。CQ、HCQ、および標準治療(SOC)が有効な比較対象となった3件の研究を除き、IVMは一般的にプラセボと比較された。IVM 12 mgを1日1回、3〜7日間、最も定期的に処方される用量です。FVP試験の追跡段階に登録された患者数は842人で、男性が圧倒的に多かった。FVPは、CQ、HCQ、およびLPV/RTVがアクティブコンパレータであった3件の研究を除き、主にSOCと比較された。FVP群の患者の場合、最も定期的に処方された用量は、1,600 mgのFVPを初日に1日2回、次の5〜14日間は1日2回600 mgでした。.追跡期間は7日から30日で、さまざまなFVP研究で実施された。すべての研究で最も頻繁に使用されたSOCは、抗生物質、抗ウイルス薬、コルチコステロイド、昇圧剤、抗凝固剤であった。
NMAは、間接的な混合治療の比較に使用されました。図2A-Dは、ネットワークグラフの概要を示しています。線の幅は、2 つのエージェントの比較に使用されるテストの数を表します。ノード サイズは、特定のエージェントにランダムに割り当てられた入院中の COVID-19 患者の数を表します。プラセボとHCQのサンプルは、このNMAで最も高いことがわかりました。
表1(A-D)は、院内死亡率、AE、回復時間、およびSpO2の改善に関するNMA比較結果をまとめたものである。主要アウトカムについては、バリシチニブによる治療により、プラセボと比較して院内死亡率が統計学的に有意に改善した(OR 0.57、95%CI:0.36〜0.92)。言い換えれば、バリシチニブを投与された人は、プラセボを投与された人と比較して、院内死亡率を経験する確率が43%低下すると推定されています。しかし、有害事象に対するIVM、FVP、LPV/RTV、またはHCQの明らかな有益性は認められていない。回復時間に関しては、IVM(MD -1.36、95%CI:-2.32〜-0.39)はプラセボよりも有益であることが判明し、プラセボと比較して回復時間が平均1.36日短縮されたことが示されました。SpO2の改善については、FVP群がIVM群よりも良好な有効性を示した(OR 1.7, 95% CI: 0.09〜3.45)。FVP群はIVM群と比較してSpO2が平均1.77単位増加した。
 |
表 1院内死亡率(A)、有害事象(B)、回復時間(C)、およびSpO2の改善(D)に対する介入のネットワークメタアナリシス結果のリーグ表 |
バリシチニブは、院内死亡率の低下に有意に優れている唯一の治療法である(図3A)。IVM、FVP、CQ、LPV/RTV、HCQ、HCQ+AZTもパフォーマンスは低下しましたが、統計的有意性はありませんでした。これらの知見は、プラセボ(SUCRA値:0.228)とIVMを最も効果の低い治療法(SUCRA値:0.351)としてランク付けするSUCRAプロットによって裏付けられています。最高ランクの治療法はバリシチニブ(SUCRA値:0.889)です。院内死亡率は、高いものから低いものへと、バリシチニブ(SUCRA値:0.889)、HCQ+AZT(SUCRA値:0.638)、SOC(SUCRA値:0.583)、LPV/RTV(SUCRA値:0.544)、HCQ(SUCRA値:0.457)、FVP(SUCRA値:0.406)、CQ(SUCRA値:0.404)、IVM(SUCRA値:0.351)、プラセボ(SUCRA値:0.228)です。SUCRAプロットではSOCが最高のパフォーマンスを発揮し、最高位にランクされる傾向がありましたが(図3B)、AEは比較に識別可能な差をもたらさなかった(SUCRA値:0.933)。SUCRAプロットでは、IVM(SUCRA値:0.583)とLPV/RTV(SUCRA値:0.519)の結果は非常によく似ています。回復時間の点では、IVMは有効性が優れているため、他の抗ウイルス薬よりも大幅に優れています(図3C)。高から低までの回復時間は、IVM(SUCRA値:0.758)、HCQ(SUCRA値:0.632)、バリシチニブ(SUCRA値:0.576)、プラセボ(SUCRA値:0.034)でした。SpO2の場合、IVMはFVPよりも有意に性能が悪い(SUCRAプロット(図3D)。SpO2の高から低への改善は、FVP(SUCRA値:0.736)、LPV/RTV(SUCRA値:0.722)、HCQ(SUCRA値:0.633)、プラセボ(SUCRA値:0.363)、IVM(SUCRA値:0.046)でした。
メタ回帰分析
4つのアウトカム(院内死亡率、有害事象、回復時間、またはSpO2の改善)すべてのメタ回帰分析を実施するために、1つの共変量(異なる治療法)が選択された。交互作用モデルに有意な係数を示す共変量はありませんでした。全ての結果を表S4に示す。
レバレッジプロット
レバレッジプロットを調べ、固定効果モデルとランダム効果モデルの逸脱度情報基準(DIC)値を比較した後、ランダム効果モデルを使用して効果サイズとCIを推定しました(図S3)。てこ比プロットは、てこ比値が小さいデータポイントの大部分が示すように、低い異質性を示しています。したがって、この研究は良好な均質性を示し、研究の異質性が低いことを示唆していると推測できます。
パブリケーションバイアス
出版バイアスは、比較のために調整されたファネルプロットを用いて検討した。肯定的な知見を報告する研究は、発表される可能性が高いという仮説を立てた。比較調整された漏斗プロットとEggerの検定を組み合わせて、小さな研究効果を検出しました(図S4)。いくつかの推定値は中心から離れていましたが、エッガーの検定P値は統計的有意性に達していないことを示しました(p=0.18、p=0.49、p=0.69、p=0.26)。
議論
本解析は、36件の研究、33,555人を7つの新規経口抗ウイルス薬に無作為に割り付けたものである。本研究で得られた知見は、COVID-19の入院患者を最適に治療するための新規経口抗ウイルス薬の選択に役立つ可能性がある。一部の抗ウイルス薬は、統計的および臨床的に異なります。院内死亡率に関しては、抗ウイルスバリシチニブを投与された研究群では、プラセボを投与された対照群と比較して、COVID-19のリスクが有意に低いことが観察されました。IVMは、回復時間の点でプラセボよりも有効でした。SpO2については、FVPは他の新規経口抗ウイルス薬よりも優れた性能を示しました。全体として、バリシチニブは、SUCRA値に基づく院内死亡率の点で他の薬剤よりも優れていることがわかりました。SpO2の回復時間とFVPにはIVMが推奨されます。また、プラセボと比較して、いずれの介入も有害事象の減少に至らなかったこともわかった。
今回の研究では、院内死亡率、有害事象、回復時間、またはSpO2の改善のアウトカムを評価することが優先された。新規経口抗ウイルス薬の臨床試験のサンプルサイズが限られているため、これらの小規模な研究からのデータの分布を分析することは困難です。バリシチニブは、抗ウイルス治療のNMA比較(SUCRA値に従って測定)から得られた知見によると、院内死亡率の低下において他の薬剤よりも優れている可能性があります。特に、バリシチニブはJAK1/JAK2を阻害して下流の炎症反応を調節し、IL-6によるSTAT3のリン酸化を用量依存的に防ぎます。29.30%SARS-CoV-2が肺胞肺細胞に侵入して感染するのを防ぐため、抗ウイルス活性があります。31このメカニズムは、COVID-19の発症にJAK-STATシグナル伝達経路が重要であるため、サイトカインバーストの減少に役立つ可能性があります。32、33 COVID-19の入院患者にバリシチニブを使用すると、死亡リスクが有意に低下した。34–37IVMは、強力な抗寄生虫作用、抗菌作用、抗ウイルス作用、抗がん作用により広く研究されている大環状ラクトン系抗寄生虫薬です。38最近の研究では、さまざまなRNAウイルスに対するIVMの抗ウイルス活性が実証されており、SARS-CoV-2に対して有効である可能性が示唆されています。39–43重症のCOVID-19におけるIVMの使用により、検査室の予後パラメータが改善され、臨床的回復が増加し、死亡率が低下しました。44対照的に、レトロスペクティブ研究では、IVMはCOVID-19患者の症状期間を短縮できなかったと報告されたが、その減少は統計学的に有意ではなかった。研究コホートが若く、併存疾患がほとんどなく、肝酵素レベルが正常の1.5倍未満であったため、結果はこのようなグループにのみ適用される可能性があります。45FVPは、ウイルス変異を誘導するウイルスRNA依存性RNAポリメラーゼの経口投与による広域スペクトル阻害剤です。46RNAウイルスの広域スペクトル抑制に対応するリン酸化誘導体(T-705RTP)は、in vivoでウイルスRNAポリメラーゼを選択的に阻害します。47.48別の研究では、FVPを投与された中等度のCOVID-19患者は、ウイルスクリアランス率が低かった。49
上記3種以外の薬剤は、強い抗ウイルス活性を示さなかった。HCQは、院内死亡率、有害事象、回復時間、またはSpO2を低下させることは示されなかった。CQがSARS-CoV-2のヒト肺細胞への侵入を阻害せず、その後の肺組織全体に拡散することを発見した最近のin vitro研究は、HCQに関するこれらの累積的な経験的結果を裏付けています。50
11月22日、塩野義製薬(株)が開発した新型コロナウイルス感染症(COVID-19)の国内内服治療剤「ゾコバ」について、新薬専門委員会(Clinicaltrials.gov の最終承認を受け、約2年にわたる審査を経て、日本政府が正式に承認しました。NCT:05305547)。経口薬は、主に米国の製薬大手メルクとファイザーによって開発されています。主に中等症の患者や重症の患者を対象としており、糖尿病、さまざまな呼吸器疾患、肥満などの重症化リスクのある患者に限定され、重症化や死亡率は低下しますが、初期症状のある患者はわずかです。日本の塩野義製薬が開発した経口薬は、特に初期症状のある人や軽度の感染症の人を対象としています。また、妊娠中の女性や特別な状態の患者を除いて、使用対象に制限はあまりありません(ClinicalTrials.gov。NCT:05605093)。風邪薬と同様に、12歳以上の人なら誰でも広く利用できます。ただし、高血圧や高脂血症など、他の36種類の薬と併用しないでください。XOCOVAの承認により、医療分野に新たな治療選択肢が加わります。そういう意味では、今まで内服薬が使えなかった人が使えるようになったのは良いことです。しかし、率直に言って、それは緊急承認された薬です。したがって、将来の新しいアップデートにご期待ください。
COVID-19の発生以来、世界中の科学者がCOVID-19に適した治療法を模索してきました。COVID-19の脅威に対抗するために、研究者は長期的なワクチン接種と短期的な予防オプションを探しています。ワクチン候補の臨床試験では大幅な改善と肯定的な結果が得られていますが、ワクチン忌避や、数百万回分から数十億回分のワクチンを大量生産して世界人口に届けるという物流上の課題など、多くの課題が残っています。51ワクチンには限界があり、新薬の生成には時間がかかるため、ウイルスや炎症性疾患に対する有効性が証明されているFDA承認の化合物がCOVID-19の治療に好まれています。しかし、COVID-19に対するこれらの薬の安全性と有効性の証明が必要であり、これは臨床試験の成功によってのみ達成できます。
重症化に向けた臨床的進歩は、患者が人工呼吸を必要とし、死亡率に直面する可能性を高めるため、患者と医療システムの両方にとって重要な意味を持ちます。さらに、COVID-19の症例が増加している時期には、この進行により、地方や地域の病院のリソースに負担がかかる可能性があります。したがって、患者が感染性ウイルスをより迅速に除去できるようにすることで、COVID-19とおそらくコミュニティ感染を減らすことが重要です。モノクローナル抗体のバムラニビマブ-エテーゼ-ビマブ、カシリビマブ-イムデビマブ、およびソトロビマブは、現在、COVID-19のリスクのある外来患者に対して承認されている治療法です。モノクローナル抗体は医療現場での輸液または注射による投与を必要とするため、診断後すぐに患者が自宅で投与できるモルヌピラビルなどの経口剤は、入院していない患者にとってより実用的で患者に優しい可能性があります。このような薬剤は、COVID-19治療の武器庫における重要な新しいツールとなるでしょう。
この研究にはいくつかの制限があることに注意する必要があります。第1に、この研究にはRCTのみが含まれており、観察研究やコホート研究は除外されているため、選択した研究の数は限られている。したがって、現在のRCTに基づくメタアナリシスにおけるエビデンスのレベルは頑健であると考えるべきである。第二に、ワクチン接種状況の影響は、治療対象集団の一般化可能性を決定する上で不可欠な要素である。SARS-CoV-2のワクチン接種率はさまざまな民族グループによって評価されているため、ワクチンを接種していない集団に対して特定の治療法が受け入れられるかどうかを慎重に評価する必要があります。選択した試験の参加者の全体的なワクチン接種状況は開示されていないが、研究のタイミングを考えると、登録された患者の大多数はワクチン未接種であった可能性が高い。第三に、私たちの研究は急性有効性/AEのみを検討し、潜在的な長期的影響についてより多くのデータを必要としました。さらに、効果サイズのCIは比較的大きく、このNMAにおける知見の信頼性に影響を与える可能性がある。最後に、抗ウイルス薬による治療が、長期にわたるCOVID-19を含むCOVID-19の長期後遺症にどのように影響するかについてのエビデンスは不明である。
COVID-19の経口抗ウイルス薬の研究は、コロナウイルス治療薬の開発と臨床応用の参考資料を提供し、将来の潜在的な感染症パンデミックの予防と対応に貢献することができます。治療ガイドラインは感染レベルの違いを反映するように更新されるべきであるが、治療介入は、患者と臨床医の臨床状況と好みを考慮して、ケースバイケースで行われるべきである。これらの知見は、患者と臨床医の意思決定の共有に寄与することが期待されます。確かに、COVID-19感染症の治療のために、より大規模なRCT/RPCTとビッグデータ解析が協力して実施されるべきである。したがって、COVID-19の予防と治療は、将来的により良い方向に変化します。
結論
要約すると、現在推奨されている抗ウイルス薬であるバリシチニブ、IVM、およびFVPは、入院中のCOVID-19患者の疾患進行予防のために継続する必要があります。これらの知見は、新たな変異株によって引き起こされる感染の波に対処するための公衆衛生対策と、ウイルスの進化に対抗するための新しい経口抗ウイルス薬の開発の重要性を浮き彫りにしている。このNMAには、当時利用可能な最高レベルの確実性が含まれていましたが、研究者にとって透明性を高めるためにデータを共有することが不可欠でした。RCTから得られた個々の患者データのメタアナリシスは、患者の特性に基づいて治療を調整するための次の論理的なステップとなる。
確認
レビュアーの皆様のご協力とご支援に感謝いたします。
著者の貢献
すべての著者は、構想、研究デザイン、実施、データ収集、分析、解釈、またはこれらすべての分野において、報告された研究に多大な貢献をしています。記事の起草、改訂、または批判的レビューに参加した。公開するバージョンに最終承認を与えた。論文が投稿されたジャーナルに合意した。そして、仕事のあらゆる側面に責任を持つことに同意しました。
融資
本研究は、鄭州市協創プロジェクト(XTCX2023006)および鄭州大学第一附属病院看護チームプロジェクト(HLKY2023005)の支援・資金提供を受けて行われました。資金提供者は、データの設計、収集、分析、出版の決定、または原稿の準備に関与していませんでした。
開示
著者らは、この作業に競合する利害関係がないことを宣言します。
参照
1. 世界保健機関(WHO)。WHO COVID-19 ダッシュボード。世界保健機関;2022. 利用可能: https://covid.19.who.int/data.2023年10月11日にアクセス。
2. Shao W, Chen X, Zheng C, 他現実世界で懸念されるSARS-CoV-2変異株に対するCOVID-19ワクチンの有効性:文献レビューとメタアナリシス。エマーグ微生物は感染します。2022;11(1):2383–2392.DOI:10.1080/22221751.2022.2122582
3. Umakanthan S, Sahu P, Ranade AV, 他コロナウイルス病2019(COVID-19)の起源、感染、診断、管理。大学院医学J.2020;96(1142):753–758.DOI:10.1136/postgradmedj-2020-138234
4. Meselson M. SARS-CoV-2の感染における液滴とエアロゾル。N Engl J Med。2020;382(21):2063.doi:10.1056/NEJMc2009324
5. Huang C, Wang Y, Li X, 他中国・武漢における2019年新型コロナウイルスに感染した患者の臨床的特徴。ランセット。2020;395(10223):497–506.doi:10.1016/S0140-6736(20)30183-5
6. Lamers MM、Haagmans BL. SARS-CoV-2の病因。ナット・レヴ・マイクロバイオール。2022;20(5):270–284.DOI:10.1038/s41579-022-00713-0
7. Wang Q, Wu J, Wang H, et al. SARS-CoV-2ポリメラーゼによるRNA複製の構造的基盤。セル。2020;182(2):417–428.e13。DOI:10.1016/j.cell.2020.05.034
8. Umakanthan S、Monice M、Mehboob S、Jones CL、Lawrence S.急性後(長期)COVID-19の生活の質:ドイツ語版(PAC19QoL)機器の検証。フロント公衆衛生。2023;11:1163360.DOI:10.3389/fpubh.2023.1163360
9. Davis HE、Assaf GS、McCorkell L、他国際コホートにおけるlong COVIDの特徴:7か月の症状とその影響。EClinicalMedicineです。2021;38:101019.DOI:10.1016/j.eclinm.2021.101019
10. Michelen M、Manoharan L、Elkheir N、他long COVIDの特徴:生きたシステマティックレビュー。BMJグロブヘルス。2021;6(9):e005427。DOI:10.1136/bmjgh-2021-005427
11. Chanda D、Hines JZ、Itoh M、Fwoloshi S、Minchella PA、Zyambo KD。ザンビアにおける院内死亡率への進行に対するCOVID-19ワクチンの有効性、2021〜2022年。オープンフォーラムは、disに感染します。2022;9(9):ofac469。DOI:10.1093/ofid/ofac469
12.中華人民共和国の国家衛生健康委員会。から入手可能: https://www.nhc.gov.cn/xcs/yqjzqk/202212/a87d93dbfbd14fc1b7837f1a20092cbe.sht.mL.2023年10月11日にアクセス。
13. Hong J, Xu XW, Yang J, 他中国東部のがん患者におけるCOVID-19ワクチンの接種意向に関する知識、態度、受容、および予測因子:横断的調査。Jインテグメッド。2022;20(1):34–44.DOI:10.1016/j.joim.2021.10.004
14. Majeed A、Molokhia M.covid-19に対する英国のワクチン接種。BMJです。2020;371:m4654です。DOI:10.1136/bmj.m4654
15. 世界保健機関(WHO)。2019年のグローバルヘルスに対する10の脅威。2019. 利用可能: https://www.who.int/news-room/spotlight/ten-threats-to-global-health-in-2019.2023年10月11日にアクセス。
16. Umakanthan S、Lawrence S.ドイツにおけるCOVID-19ワクチン忌避の予測因子:横断的な人口ベースの研究。大学院医学J.2022;98(1164):756–764.DOI:10.1136/postgradmedj-2021-141365
17. Umakanthan S、Bukelo MM、Bukelo MJ、Patil S、Subramaniam N、Sharma R.インドにおけるCOVID-19ワクチン忌避の社会環境予測因子:人口ベースの調査。ワクチン。2022;10(10):1749.DOI:10.3390/vaccines10101749
18.クリスティA、Mbaeyi SA、ワレンスキーRP。ワクチン接種完了者に対するCDCの暫定勧告:重要な第一歩。ジャマ。2021;325(15):1501–1502.DOI:10.1001/jama.2021.4367
19.国立衛生研究所。管理。COVID-19治療ガイドライン。から入手可能: https://www.covid19.treatment.guidelines.nih.gov/ma-nagement/.2023年10月11日にアクセス。
20. Kumari M, Lu RM, Li MC, et al.COVID-19の現在の進歩の重要な概要:ワクチン、抗ウイルス薬、および治療用抗体の開発。Jバイオメッドサイ。2022;29(1):68.DOI:10.1186/s12929-022-00852-9
21.ファーナーRE、アロンソンJK。covid-19のレムデシビル。BMJです。2020;369:M1610です。DOI:10.1136/bmj.m1610
22. Drożdżal S、Rosik J、Lechowicz K、他SARS-CoV-2(COVID-19)治療薬の治療薬に関する最新情報。薬剤はUpdatに抵抗します。2021;59:100794.DOI:10.1016/j.drup.2021.100794
23. Page MJ, McKenzie JE, Bossuyt PM, 他PRISMA 2020ステートメント:システマティックレビューを報告するための更新されたガイドライン。Inter J Surg.2021;88:105906.DOI:10.1136/bmj.n71
24. Xu C、Niu Y、Wu J、Gu H、Zhang C.ネットワークメタ分析のためのソフトウェアとパッケージの適用:使用法ベースの比較研究。J Evid ベースの Med.2018;11(3):176–183.DOI:10.1111/jebm.12264
25.シムS、ユンBH、シンIS、ペJM。ネットワークメタアナリシス:Stataを使用したアプリケーションと実践。エピデミオールの健康。2017;39:e2017047です。DOI:10.4178/epih.e2017047
26. Béliveau A, Boyne DJ, Slater J, Brenner D, Arora P. BUGSnet: ベイジアンネットワークメタアナリシスの実施と報告を容易にするためのRパッケージ。BMC med res methodol.2019;19(1):196.DOI:10.1186/s12874-019-0829-2
27. Wan X、Wang W、Liu J、Tong T.サンプルサイズ、中央値、範囲、および/または四分位範囲からサンプル平均と標準偏差を推定します。BMC med res methodol.2014;14:135.DOI:10.1186/1471-2288-14-135
28.ヒギンズJPT、アルトマンDG。選択した研究におけるバイアスのリスクの評価。コクランハンドブックSyst Rev Inter.2011;2011:187–241.
29. Bronte V、Ugel S、Tinazzi E、他バリシチニブは、重症のCOVID-19患者の免疫調節不全を抑制します。Jクリン投資。2020;130(12):6409–6416.DOI:10.1172/JCI141772
30. Cherian JJ、Eerike M、Bagepally BS、Das S、Panda S.COVID-19の入院患者におけるバリシチニブとトシリズマブの有効性と安全性:システマティックレビューとメタアナリシスを使用した比較。フロントファーマコール。2022;13:1004308.DOI:10.3389/fphar.2022.1004308
31. McInnes IB、Byers NL、Higgs REなどバリシチニブ、ウパダシチニブ、およびトファシチニブを介したヒト白血球亜集団におけるサイトカインシグナル伝達の調節の比較。関節炎resther。2019;21(1):183.DOI:10.1186/s13075-019-1964-1
32.リチャードソンP、グリフィンI、タッカーC、他。2019-nCoV急性呼吸器疾患の潜在的な治療法としてのバリシチニブ。ランセット。2020;395(10223):e30–e31。DOI:10.1016/S0140-6736(20)30304-4
33. Hoang TN、Pino M、Boddapati AK、他バリシチニブ治療は、SARS-CoV-2に感染したアカゲザルの下気道マクロファージの炎症と好中球の動員を解決します。セル。2021;184(2):460–475.e21。DOI:10.1016/j.cell.2020.11.007
34. 米国食品医薬品局。米国食品医薬品局;2022. 利用可能: https://www.fda.gov/media/143822/download.2023年10月11日にアクセス。
35.RECOVERYコラボレーショングループ。COVID-19で入院した患者におけるバリシチニブ(回復):無作為化、対照、非盲検、プラットフォーム試験、および更新されたメタアナリシス。ランセット。2022;400(10349):359–368.doi:10.1016/S0140-6736(22)01109-6
36. Marconi VC、Ramanan AV、de Bono SなどCOVID-19の入院成人の治療に対するバリシチニブの有効性と安全性(COV-BARRIER):無作為化、二重盲検、並行群間、プラセボ対照第3相試験。ランセット呼吸薬。2021;9(12):1407–1418.DOI:10.1016/S2213-2600(21)00331-3
37. Cantini F、Niccoli L、Matarrese D、Nicastri E、Stobbione P、Goletti D. COVID-19におけるバリシチニブ療法:安全性と臨床的影響に関するパイロット研究。J感染。2020;81(2):318–356.DOI:10.1016/j.jinf.2020.04.017
38. Awad H、Hassan B、Dweek S、Aboelata Y、Rawas-Qalaji M、Ahmed IS。COVID-19の治療および/または予防のための抗寄生虫薬イベルメクチンの転用の可能性。医薬品。2022;15(9):1068.DOI:10.3390/ph15091068
39. Formiga FR、Leblanc R、de Souza Rebouças J、Farias LP、de Oliveira RN、Pena L.イベルメクチン:COVID-19に対する抗ウイルス活性が期待される受賞歴のある薬。Jコントロールリリース。2021;329:758–761.DOI:10.1016/j.jconrel.2020.10.009
40. Krolewiecki A、Lifschitz A、Moragas MなどCOVID-19の成人における高用量イベルメクチンの抗ウイルス効果:概念実証無作為化試験。EClinicalMedicineです。2021;37:100959.DOI:10.1016/j.eclinm.2021.100959
41. Rakedzon S、Neuberger A、Domb AJ、Petersiel N、Schwartz E.ヒドロキシクロロキンからイベルメクチンまで:SARS-CoV-2と戦うための抗寄生虫薬の抗ウイルス特性は何ですか?Jトラベルメッド。2021;28(2):TAAB005。DOI:10.1093/jtm/taab005
42.カリーL、ドルースJD、キャットンMG、ヤンスDA、ワグスタッフKM。FDA承認薬イベルメクチンは、in vitroでSARS-CoV-2の複製を阻害します。抗ウイルス剤2020;178:104787.DOI:10.1016/j.antiviral.2020.104787
43. Okumuş N、Demirtürk N、Çetinkaya RAなど。重症のCOVID-19患者の治療にイベルメクチンを追加することの有効性と安全性の評価。BMC Infect Dis. (BMC 感染ディス)2021;21(1):411.DOI:10.1186/s12879-021-06104-9
44. Jean SS、Hsueh PR.COVID-19の治療のための古い薬と再利用された薬。エキスパートRevアンチインフェクトサー。2020;18(9):843–847.DOI:10.1080/14787210.2020.1771181
45. López-Medina E、López P、Hurtado IC、他軽度のCOVID-19成人の症状の解決までの時間に対するイベルメクチンの効果:無作為化臨床試験。ジャマ。2021;325(14):142 6–1435.DOI:10.1001/jama.2021.3071
46. Hung DT、Ghula S、Aziz JMAなどCOVID-19患者に対するファビピラビルの有効性と有害作用:発表された臨床試験と観察研究の系統的レビューとメタアナリシス。int j infect dis.2022;120:217–227.DOI:10.1016/j.ijid.2022.04.035
47. 土井泰彦、日比野雅之、長谷亮、他COVID-19の入院患者を対象としたファビピラビル療法の早期および後期の前向き無作為化非盲検試験。抗菌剤ケマザー。2020;64(12):e01897–20。doi:10.1128/AAC.01897-20
48. 古田 泰彦, Gowen BB, 高橋 和彦, 白木 和彦, Smee DF, Barnard DL.ファビピラビル(T-705)、新規ウイルスRNAポリメラーゼ阻害剤。抗ウイルス剤2013;100(2):446–454.DOI:10.1016/j.antiviral.2013.09.015
49.ワシチェンコI、A。2019年中等度のコロナウイルス病(COVID-19)患者の治療のためのアビファビル:第II/III相多施設無作為化臨床試験の中間結果。Clin Infect Dis.2021;73(3):531–534.DOI:10.1093/cid/ciaa1176
50. Hoffmann M、Mösbauer K、Hofmann-Winkler Hなど。クロロキンは、SARS-CoV-2によるヒト肺細胞の感染を阻害しません。自然。2020;585(7826):588–590.DOI:10.1038/s41586-020-2575-3
51. Umakanthan S、Patil S、Subramaniam N、Sharma R.人口ベースの縦断調査を通じて調査されたインドにおけるCOVID-19ワクチンの躊躇と抵抗。ワクチン。2021;9(10):1064.DOI:10.3390/vaccines9101064
















 PAGE TOP
PAGE TOP
この記事へのコメントはありません。